知识库
抗体偶联药物(ADC)为什么这么火?资本押注的底层逻辑
近年来,全球生物医药领域热度最高、资本集中度最强的赛道,非抗体偶联药物(ADC)莫属。从跨国药企天价并购,到本土创新药企业频频刷新License-out纪录,再到一级市场融资持续火热,ADC早已不是小众前沿技术,而是成为肿瘤治疗领域的核心支柱。
其实在往期的文章中,小编已经和大家分享过小核酸药物、细胞基因治疗两大热门赛道的深度解析,它们与ADC一同构成了当前生物医药领域创新突围的三大核心方向。相较于小核算的精准调控、细胞基因治疗的根治潜力,ADC凭借“精准靶向+强效杀伤”的独特优势,成为资本布局最密集、临床转化最快速的赛道之一。
一、ADC 概念详解
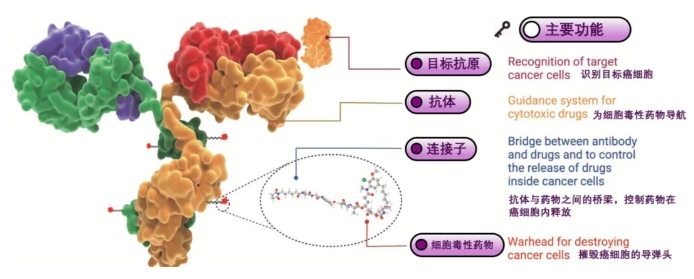
ADC,全称是抗体药物偶联物(Antibody-Drug Conjugate),简单说就是把单克隆抗体、高效杀肿瘤药物,通过连接子连接在一起的新型靶向药。它最核心的好处就是能“精准杀肿瘤”,就像一枚精准制导的“生物导弹”,各个部分分工明确、配合工作,既能有效杀死肿瘤细胞,又能最大程度减少对正常细胞的伤害。
具体来说,ADC的三个核心部分,作用分别是:
抗体部分:相当于“导弹的导航”,专门找肿瘤细胞。肿瘤细胞表面有正常细胞没有或很少有的特殊标记(抗原),抗体能精准识别并抓住这个标记,锁定肿瘤细胞,不会误伤到正常细胞。
连接子:相当于“导弹的引爆开关”,一边连抗体、一边连杀肿瘤药物。它在血液里很稳定,不会让药物提前释放伤害正常组织;等ADC被肿瘤细胞“吞”进去后,连接子就会断裂,把杀肿瘤药物释放出来。
细胞毒性药物:相当于“导弹的弹头”,杀肿瘤的能力很强。这种药如果单独用,毒性太大,会伤害很多正常细胞;但和抗体、连接子连在一起后,能精准送到肿瘤细胞里,只在肿瘤部位发挥作用,大大减少对全身的副作用。
总的来说,ADC结合了抗体“精准找肿瘤”和化疗药“强力杀肿瘤”的优点,解决了传统化疗“杀肿瘤的同时也伤正常细胞”的问题。现在它在乳腺癌、肺癌、血液肿瘤、胃癌等肿瘤治疗中用得越来越多,也是目前生物医药领域的热门研究方向和重要治疗方法。
二、ADC市场空间
判断一个赛道的投资价值,首先要看市场空间的广度与增长潜力——ADC赛道的答案,无疑是“爆发式增长”。
截至026年,全球已有21款ADC药物获批上市,覆盖乳腺癌、淋巴瘤、肺癌等12类实体瘤及血液瘤,市场规模突破200亿美元。
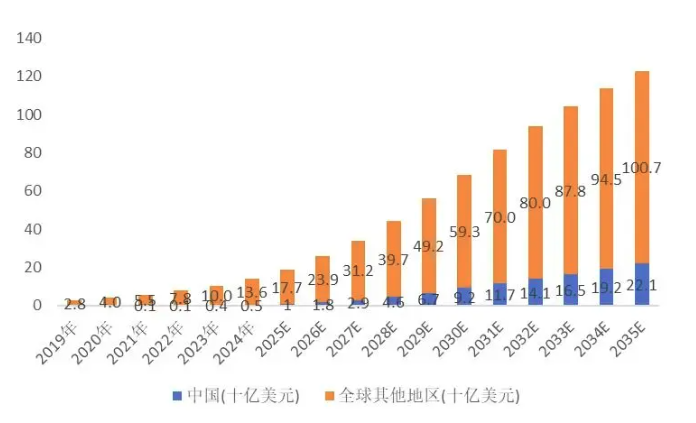
全球 ADC 市场由 2019 年的 28 亿美元增长至 2024 年的 141 亿美元,复合年增长率达 37.9%;预计 2030 年将增至 685 亿美元,2035 年突破 1227 亿美元,2024—2030 年、2030—2035 年复合年增长率分别为 30.1%、12.4%。
中国市场增长更为迅猛,规模从 2024 年的 5 亿美元预计增至 2030 年的 92 亿美元,复合年增长率高达 60.1%;2035 年将进一步升至 221 亿美元。
更值得关注的是适应症的持续拓展,ADC已从晚期后线治疗,逐渐向早期一线、新辅助/辅助治疗前移,覆盖乳腺癌、肺癌、胃癌、尿路上皮癌、血液肿瘤等多个主流瘤种,临床需求不断扩容,为市场增长提供了持续动力。
三、技术与管线
对于生物医药赛道,技术壁垒和管线质量是决定企业估值的核心,ADC也不例外。ADC的核心构成的是“抗体+连接子+细胞毒性药物”,三者的协同优化,构成了不同代际ADC的竞争力差异,也决定了投资价值的高低。
(一)四代技术演进路径
从发展历程来看,ADC已从第一代发展至第四代,每一次迭代都带来疗效和安全性的显著提升:
第一代ADC药物:
代表药物为Mylotarg(吉妥珠单抗),这是2000年FDA批准的第一款ADC药物,用于治疗急性髓系白血病,后因严重致命肝损伤且无明显生存获益,于2010年自愿退出市场,2017年重新上市。药物设计始于1958年,尝试用抗小鼠白细胞免疫球蛋白与甲氨蝶呤联合治疗白血病,
核心缺点突出:抗体为鼠抗体、连接子不可切割、细胞毒素效力不足,导致脱靶毒性高、药效低,多数产品以失败告终,目前已基本被淘汰,投资价值极低。
第二代ADC药物:
以Kadcyla(T-DM1)、Adcetris为代表,其中Kadcyla是首个获批用于乳腺癌的ADC药物,Adcetris则在经典霍奇金淋巴瘤和间变性大细胞淋巴瘤领域表现突出。这一代在技术上有所改进,采用人源化抗体提升靶向性、减少交叉反应,开发多样化靶抗原,引入可切割连接子技术,但仍存在明显短板:采用传统化学偶联方法,药物抗体比(DAR)均匀性差,连接子在血液中易裂解,载药率不稳定,治疗窗口窄、有效性不足,天花板较低,投资价值中等。
第三代ADC药物:
当前市场主流,代表药物包括Enhertu(DS-8201)、Besponsa、Padcev、维迪西妥单抗等,其中Padcev是第二种靶向实体瘤的ADC药物,适用于PD-1/PD-L1抗体治疗失败的患者。在前三代基础上,采用位点特异性偶联技术,实现DAR值均匀,改用完全人源化抗体降低免疫原性,同时优化连接子和载荷,大幅降低脱靶毒性、提升药代动力学效率。其优势在于小分子单抗位点特异性偶联、双特异性抗体开发等,缺点是偶联技术难以重现、对微管蛋白抑制剂不敏感,该代产品已通过临床和商业化验证,投资价值最高。
第四代ADC药物:
向双抗ADC、条件激活型、免疫刺激型(ISAC)等方向突破,代表药物有DS-8201、Trodelvy、SKB264等。核心改进的是载荷采用拓扑异构酶I抑制剂(喜树碱衍生物),设计为低毒性、高效力,DAR值维持在7.4-7.8之间,可向肿瘤细胞递送更多有效载荷。但仍有优化空间:载荷机理单一、易产生耐药性,连接子在循环系统中稳定性不足,ADC分子量大、肿瘤富集速度慢、通透性低,抗体选择受限。该代技术壁垒高,具备First-in-class潜力,是未来创新方向,投资回报预期高,例如百利天恒的BL-B01D1,已成为全球首个申报上市的双抗ADC。
(二)四大核心技术壁垒
1. 靶点选择:当前靶点竞争格局呈现“C-MET崛起、HER2持续火热”的特点,整体靶点分布TOP5为C-MET(180个研究)、HER2(105个研究)、CD30(32个研究)、TROP2(15个研究)、FOLR1(13个研究);其中成熟靶点(HER2、TROP2、Nectin-4)竞争激烈,而新兴靶点(Claudin18.2、B7-H3、HER3、C-MET、FOLR1等)具备差异化优势,能获得更高的估值溢价。
2. 连接子技术:其稳定性与药物释放效率,直接决定ADC的毒性与疗效,是核心竞争力之一,未来新型连接子技术将聚焦提高稳定性和肿瘤选择性释放。
3.载荷开发:载荷,效力、旁观者效应、免疫原性是关键,直接影响肿瘤杀伤效果,未来将重点开发作用机制不同的新型细胞毒性载荷,以克服耐药性;
4.偶联工艺:定点偶联相比随机偶联,能实现DAR均一、质量可控,是企业工艺实力的核心体现,也是规模化生产的关键。
(三)管线布局逻辑
从管线布局逻辑来看,资本更青睐“厚度+差异化+进度”三者兼具的企业。当前ADC临床开发仍以早期研究为主,I期及I期推断研究占41.3%,II期占8.3%,III期仅占1.4%,大量新型ADC分子处于早期开发阶段。
具体布局策略上,一是避开HER2、TROP2等红海靶点,布局Claudin18.2(适配胃癌、胰腺癌等中国高发肿瘤)、B7-H3(适配泛实体瘤)、C-MET、FOLR1等细分赛道,其中C-MET已成为绝对热门靶点,国际药企开展25个相关研究,本土药企更是达到28个,凸显本土企业对新兴靶点的高度重视;
二是聚焦中国特色瘤种(胃癌、肝癌、食管癌),打造全球竞争力,本土药企在HER2靶点上开展25个研究,重点聚焦乳腺癌、胃癌等本土高发肿瘤;
三是探索ADC与PD-1/PD-L1的联用策略,这一组合已在多个临床试验中验证可协同增强抗肿瘤效应,有望在2028年后替代IO+化疗,实现市场空间翻倍,
四是ADC向自身免疫病(红斑狼疮、类风湿关节炎)的延伸,打开千亿级新市场,同时向血液肿瘤拓展,尤其是多发性骨髓瘤、淋巴瘤领域将成为新的研发热点;五是布局双特异性ADC等前沿方向,通过同时靶向两个肿瘤相关抗原,提高特异性,打造差异化优势。
四、竞争格局
全球 ADC 赛道呈现头部集中、梯队分明格局,跨国药企凭借资金、研发与商业化能力占据主导,而中国企业凭借靶点创新、成本优势与出海能力快速崛起,两者形成互补竞争、共同推动赛道发展的态势,成为全球肿瘤药领域最具活力的赛道之一。
头部企业中,罗氏、阿斯利康、吉利德等跨国药企稳居第一梯队,CR5市占率超68%,牢牢掌控着全球ADC市场的主导权。这些企业凭借数十年的研发积累、雄厚的资金实力,全面掌控抗体、连接子、毒素三大核心环节的核心技术,构建起难以突破的专利壁垒。同时,它们依托覆盖全球主要市场的成熟商业化网络,推动新品快速实现全球落地,凭借高定价策略抢占高端市场。
而中国企业则凭借差异化优势快速突围,涌现出一批实力突出的龙头企业。
百济神州全球化商业化能力行业领先,这一优势为其ADC领域布局提供了坚实支撑。公司已搭建起覆盖全球主要市场的商业化体系,临床开发、注册申报与供应链能力同步成熟,能够高效推动ADC产品的全球落地与推广。目前,百济神州在ADC领域有深度布局,依托自身成熟的全球化资源,在ADC前沿赛道稳步推进,助力国产ADC产品参与全球市场竞争。
荣昌生物走清晰的差异化创新之路,核心聚焦ADC领域,拥有维迪西妥单抗这一中国首款原创ADC药物,这一产品的推出填补了国产原创ADC领域的空白,彰显了公司在ADC领域的创新实力。围绕维迪西妥单抗这一ADC核心产品,公司形成“国内销售+海外授权”双轮驱动模式,通过国内市场化放量与海外授权合作,推动国产原创ADC药物的市场化与国际化发展,进一步巩固其在ADC领域的差异化优势。
百利天恒以ADC领域为核心发展方向,重点布局iza-bren(EGFR×HER3双抗ADC),该产品是国产双抗ADC出海的重要里程碑,标志着国产双抗ADC获得全球市场认可。2023年,公司与BMS就该ADC产品达成总金额最高达84亿美元的合作,创下国产双抗ADC海外授权的高额纪录。目前,该ADC产品两项适应症已获CDE受理并纳入优先审评,全球II/III期临床试验同步推进,公司拥有的中美两地研发中心,为ADC领域的源头创新提供了强有力的技术支撑,助力其持续推进ADC产品的研发与全球化布局。
三家企业分别以全球化商业化、差异化源头创新、高端双抗 ADC 出海为核心优势,代表中国 ADC 赛道从仿制走向原创、从本土走向全球的跨越式发展,也构成了中国创新药在全球 ADC 竞争中的核心力量,为后续产品全球化落地奠定坚实基础。
五、总结与展望
作为肿瘤治疗领域的 “生物导弹”,ADC 药物凭借精准靶向与强效杀伤的双重优势,已从前沿技术彻底成长为抗肿瘤市场的核心支柱。全球市场持续高速增长,中国市场更是以远超全球的增速快速崛起,成为驱动行业发展的关键引擎。
未来,随着适应症不断向早期一线、泛癌种乃至自身免疫疾病延伸,叠加联合治疗方案的逐步成熟,ADC 赛道仍具备巨大的增长空间与想象空间。对于投资者与行业参与者而言,兼具技术壁垒、管线差异化与全球化能力的企业,将在新一轮行业浪潮中占据先机;而国产 ADC 也将凭借持续创新,在全球肿瘤药物市场中占据越来越重要的位置,真正实现中国创新药的全球化突围。
【声明】
植众德本通过其官方网站http://www.meritsip.com/
提供更多相关信息。本文内容由植众德本小编从公开网络平台收集,版权归植众德本所有。未经植众德本授权,任何单位或个人不得转载本文内容。已获授权的,应在授权范围内使用,并注明来源。对于任何侵犯版权或信息错误的情况,植众德本将及时进行处理,并追究相关法律责任。授权相关事宜请联系:meritsip@meritsandtree.com。
合作对接通道!
如果您是投资机构、医药 / 器械上市公司、海外 BD 团队、产业合作伙伴,对投融资项目感兴趣,欢迎扫描下方二维码添加微信,共抓医疗健康领域创新机遇!

欢迎扫码 · 联系我们