知识库
11 款有望成为重磅炸弹或改变现有治疗范式的新药!
日前,近期,权威机构科睿唯安发布《Drugs to Watch™ 2026》报告,聚焦今年有望获批或刚上市的 11 款创新疗法。这些药物瞄准肥胖、肿瘤、基因治疗等领域,预计五年内成长为 “重磅品种”,将重塑细分赛道的市场格局。
报告预测,2035 年全球肥胖症药物市场规模将突破 1500 亿美元。其中,GLP-1 受体激动剂类药物正进入 “迭代成熟期”—— 研发方向集中在 “口服剂型突破”“多激素机制探索”“合并症场景拓展” 三大方向,通过差异化策略解决现有药物的耐受性问题,并借助联合疗法实现 “长期体重控制”。
而在罕见病领域,全球已确诊的 7000 余种罕见病中,仅约 500 种有获批疗法。当前研发已从肿瘤领域向外延伸,覆盖神经、精神、血液等系统;同时,靶向蛋白降解剂、口服免疫制剂等新技术,正推动肿瘤与免疫领域的 “精准治疗革命”。
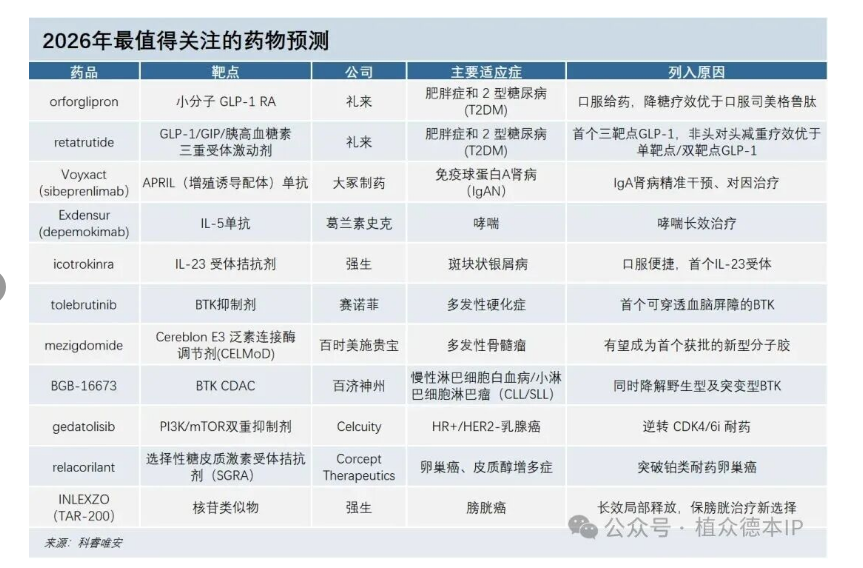
本次入选的药物需满足 “处于 II/III 期临床、预注册、注册阶段,或 2026 年初上市” 的条件。报告结合 “销售额预测、临床研发趋势、专家评估” 等维度,最终选出 11 款值得关注的候选药物。以下为各个药物的具体详情信息。
01 Orforglipron
在科睿唯安这份榜单中,礼来研发的 Orforglipron 位居首位,其核心突破在于成为全球首个进入 III 期临床试验的口服非肽类小分子 GLP-1 受体激动剂(GLP-1 RA),主要适用于超重 / 肥胖及 2 型糖尿病(T2DM)的治疗。对于全球超 2.5 亿肥胖症患者而言,这款药物有望成为极具变革性的疗法 —— 显著提升用药可及性与治疗耐受性,破解当前临床治疗中的关键痛点。
相较于诺和诺德旗下的肽类口服司美格鲁肽,Orforglipron 在给药便捷性上形成明显优势。诺和诺德的司美格鲁肽对给药条件有着严格限制,患者需空腹服用,且饮食与饮水量均受约束,这一特性直接导致患者用药依从性普遍偏低;而 Orforglipron 的口服方式更为灵活,无需受上述条件限制。不仅如此,作为小分子药物,Orforglipron 还具备生产工艺简化、生产成本更低的特点,且无需冷藏储存,这一核心优势将大幅降低药物的推广与使用门槛,为 GLP-1 RA 疗法在全球范围内的普及奠定基础。
值得行业重点关注的是,礼来此前对外披露了 III 期临床试验 ATTAIN-MAINTAIN 的关键阳性数据。该试验的核心研究目标,是评估患者经司美格鲁肽(Wegovy)和替尔泊肽(Zepbound)初始减重治疗后,采用 Orforglipron 维持体重的实际效果。试验结果显示,与安慰剂组相比,Orforglipron 不仅成功达成试验预设的主要终点,还顺利满足所有关键次要终点;尤其在患者配合健康饮食与体育锻炼的前提下,其体重维持效果显著优于安慰剂。基于这一优异的临床数据,礼来已正式向美国 FDA 递交 Orforglipron 用于成人肥胖或超重治疗的新药上市申请(NDA),且同步获得了 FDA 授予的局长优先审评券(CNPV),这将有效缩短药物审批周期,加速其落地进程。
02 Retatrutide
礼来另一款肥胖症新药 Retatrutide 同样跻身榜单,其核心突破在于有望成为全球首个靶向 GLP-1、GIP、胰高血糖素的三重受体激动剂 —— 通过同时调控多条代谢通路,相较替尔泊肽(Mounjaro/Zepbound)等现有疗法,具备实现更全面代谢调节效果的潜力,是当前肥胖症治疗领域机制创新的代表性品种。
科睿唯安预测,2031 年该药物在 G7 市场的肥胖症适应症销售额将达 100 亿美元,2 型糖尿病适应症销售额可达 201 亿美元,两大核心适应症合计市场规模突破 300 亿美元,展现出极强的商业价值。
临床数据方面,Retatrutide 在肥胖适应症 II 期试验中创下行业纪录:所有受试者体重降幅均不低于 5%,治疗 48 周时平均减重 24.2%,达到 “手术级减重” 标准;其中最高剂量组约 25% 的患者减重幅度超 30%,大幅超越现有 GLP-1 类药物的临床表现。此外,其针对肥胖 / 超重人群的 III 期试验进一步显示,该药物在实现显著减重的同时,可同步缓解患者的膝骨关节炎疼痛,为肥胖合并骨关节炎的患者提供了 “减重 + 镇痛” 的双重获益方案。
03 Depemokimab
葛兰素史克(GSK)研发的 Depemokimab 是一款靶向白介素 - 5(IL-5)的单克隆抗体类创新药,核心适应症为青少年及成人哮喘,其差异化优势在于采用 “每半年皮下注射一次” 的长效给药方案,大幅降低患者用药频率,是当前哮喘治疗领域提升依从性的代表性品种。
2025 年 12 月,该药物同步在英国与美国获批上市,获批适应症聚焦 “12 岁及以上伴有嗜酸性粒细胞表型的重度哮喘患者的附加维持治疗”,精准覆盖了哮喘亚型中临床需求未被充分满足的群体。
从市场维度看,G7 地区中重度哮喘患者规模已达 1440 万人,科睿唯安预测,Depemokimab 在该区域的销售额将于 2031 年达到 5.1 亿美元。临床数据层面,GSK 为其开展的多项确证性 III 期试验均成功达到主要终点,为药物的疗效与安全性提供了扎实支撑。
目前,GSK 正推进 Depemokimab 的适应症拓展布局,将其应用范围延伸至慢性鼻窦炎伴鼻息肉(CRSwNP)、嗜酸性肉芽肿性多血管炎(EGPA)及高嗜酸性粒细胞综合征等 IL-5 介导的疾病领域,有望通过 “一药多适应症” 的策略,进一步挖掘其临床价值与市场潜力。
04 Icotrokinra
强生研发的 Icotrokinra 是自身免疫性疾病治疗领域的关键候选药,核心突破在于有望成为全球首款获批的口服肽类 IL-23 受体阻断剂。IL-23 受体是中重度斑块状银屑病、溃疡性结肠炎等疾病炎症反应的核心驱动靶点,其靶向阻断对疾病进展控制至关重要,而该药的口服剂型将填补同类药物给药方式的空白。
该药采用每日一次口服的给药方案,显著提升患者依从性。在针对中重度斑块状银屑病的两项 III 期临床研究(ICONIC-ADVANCE 1 和 2)中,均取得关键阳性结果,顺利达成共同主要终点。核心试验数据显示其疗效优于当前主流药物氘可来昔替尼(颂狄多):治疗第 24 周时,50% 患者达到银屑病面积和严重程度指数改善 90%(PASI 90)的高标准,近半数患者实现皮肤完全清除,临床获益显著。
科睿唯安采访的行业 KOL 指出,Icotrokinra 凭借口服便捷性优势,将重塑银屑病治疗格局。2025 年 G7 市场斑块状银屑病确诊患者达 1170 万人,报告预测 2034 年该药或成为该领域处方量最高的药物,2031 年销售额将达 15 亿美元。值得关注的是,2017 年强生与 Protagonist Therapeutics 以 9.9 亿美元达成合作,获得该药所有适应症的许可与商业化权益,为其研发推进奠定基础。
05 Sibeprenlimab
大塚制药研发的 Sibeprenlimab( Voyxact)作为全球首款选择性增殖诱导配体(APRIL)抑制剂,在 IgA 肾病(IgAN)治疗领域具有里程碑意义,有望成为该领域核心的疾病修饰类药物,填补临床治疗空白。
IgA 肾病是一种进展性自身免疫性疾病,病情呈进行性发展,最终易导致肾衰竭,患者需依赖透析维持生命,临床需求极为迫切。Sibeprenlimab 采用每 4 周皮下注射一次的给药方案,通过精准靶向 IgA 肾病发病机制中的核心驱动因子 APRIL,直击疾病根源,核心作用是显著降低患者蛋白尿水平,从而延缓疾病进展。
基于 III 期 VISIONARY 临床试验的显著疗效数据,美国 FDA 于 2025 年 11 月对其授予加速批准。该试验结果显示,与安慰剂组相比,Sibeprenlimab 可显著降低患者 24 小时尿蛋白 / 肌酐比值(UPCR),且降幅兼具统计学意义与临床价值,为其疗效提供了扎实的循证医学支撑。目前,该药的适应症拓展稳步推进,针对干燥综合征的临床试验已在开展中。
06 Tolebrutinib
赛诺菲研发的 Tolebrutinib 是一款具备血脑屏障穿透能力的布鲁顿酪氨酸激酶(BTK)抑制剂,核心适应症聚焦非复发性继发进展型多发性硬化症(nrSP-MS)。与传统仅能抑制外周炎症的治疗药物相比,该药凭借创新作用机制形成显著差异化优势,可直接作用于进展型多发性硬化症的核心炎症通路,有望延缓神经退行性病变及残疾累积进程,为 nrSP-MS 这一高度未满足医疗需求的疾病提供突破性治疗方案。
然而,该药的审批进程遭遇重大波折:2025 年 12 月,美国 FDA 向赛诺菲发出完整回复函(CRL),拒绝其上市申请。赛诺菲明确表示,该决定与 FDA 此前的反馈存在 “重大且实质性的转向”,而 FDA 公开的 CRL 全文显示,核心否决原因是经评估,Tolebrutinib 在所有试验人群中的风险获益比未达到可接受水平。
从临床数据来看,Tolebrutinib 的表现呈现明显的 “喜忧参半” 态势:针对 nrSP-MS 的 III 期 HERCULES 试验成功达到主要终点,清晰展现出延缓患者残疾进展的积极疗效;但另一项 III 期 PERSEU 试验及 GEMINI 试验均未达成主要研究终点,导致其整体临床证据链存在短板。目前,赛诺菲正等待 FDA 的进一步指导意见,以明确后续研发与审批的推进方向。
07 Gedatolisib
Celcuity 研发的 Gedatolisib 是一款潜在同类首创的泛 PI3K/mTOR 抑制剂,核心定位为攻克 HR+/HER2 - 转移性乳腺癌患者对标准内分泌治疗的耐药难题,填补该领域临床治疗空白。
III 期 VIKTORIA-1 研究数据为其疗效提供了关键支撑:在 PIK3CA 野生型 HR+/HER2 - 晚期乳腺癌二线治疗场景中,Gedatolisib 展现出突出的临床优势,相较于现有治疗方案竞争力显著,成为该细分领域极具潜力的候选药物。需注意的是,HR+/HER2 - 乳腺癌是乳腺癌整体市场的最大亚型,临床需求缺口显著,仅其耐药后治疗的适应症市场规模就达数十亿美元。
从市场前景来看,HR+/HER2 - 乳腺癌全球市场规模增长强劲,预计将从 2024 年的 165 亿美元攀升至 2030 年的峰值 378 亿美元。依托这一广阔市场基础,科睿唯安预测,2031 年 Gedatolisib 在 G7 市场的销售额将达 10.8 亿美元。
为进一步挖掘药物价值,Celcuity 正同步推进 Gedatolisib 的适应症拓展,目前已启动针对转移性去势抵抗性前列腺癌(mCRPC)的临床试验,有望通过 “一药多适应症” 策略扩大其市场覆盖范围,提升商业潜力。
08 INLEXZO
强生旗下 INLEXZO(通用名:TAR-200)是一款针对高危非肌层浸润性膀胱癌(NMIBC)的创新给药系统,核心适应症聚焦对卡介苗(BCG)无反应、伴有原位癌(CIS)(伴或不伴乳头状肿瘤)的患者,填补了该类患者的治疗空白。其审批进程展现出显著优势:2025 年 7 月获美国 FDA 优先审评资格,同年 9 月便成功获批上市,审批周期不足两个月,凸显其临床价值与紧迫性。
作为全球首款实现抗癌药物向膀胱内长效局部递送的给药系统,INLEXZO 以抗代谢类核苷类似物为活性成分,依托专属 TAR-200 给药系统实现膀胱内精准灌注。该设计可提升药物在膀胱局部的浓度与作用时长,同时减少全身暴露带来的不良反应,体现出精准治疗的核心思路。其临床给药方案采用 “诱导 + 维持” 两阶段模式:诱导治疗阶段每 3 周给药一次,快速控制病情;维持治疗阶段调整为每 12 周给药一次,在保障疗效的同时降低给药频率,提升患者依从性。
从市场潜力来看,高危 NMIBC 患者存在显著未满足需求,科睿唯安报告预测,2031 年 INLEXZO 在 G7 市场的销售额将达 18 亿美元,有望成为该领域的核心治疗药物,为膀胱癌精准治疗领域带来重要突破。
09 Relacorilant
2025年12月31日,Corcept Therapeutics 遭遇重大研发挫折 —— 美国 FDA 针对其 relacorilant 用于治疗库欣综合征所致高血压的新药上市申请,发出完整回复函(CRL)并予以拒绝,直接导致该公司原计划 2026 年推动该药两项适应症同步获批的战略目标落空。
面对这一局面,Corcept 迅速调整研发重心,将核心资源转向 relacorilant 治疗铂耐药卵巢癌的适应症,目前该适应症的上市申请已进入关键阶段,PDUFA 日期设定为 2026 年 7 月,为药物后续获批划定了明确时间节点。支撑这一研发转向的核心依据是关键性 III 期 ROSELLA 临床试验的阳性数据:与单药白蛋白结合型紫杉醇治疗方案相比,relacorilant 联合白蛋白结合型紫杉醇的联合疗法,显著延长了铂耐药卵巢癌患者的无进展生存期(PFS)这一核心主要终点,联合治疗组患者 PFS 达 6.5 个月,而单药组仅为 5.5 个月,展现出明确的临床获益优势。
尽管库欣综合征相关适应症遇阻,但铂耐药卵巢癌领域的积极数据为 relacorilant 带来了新的市场机遇。科睿唯安报告预测,凭借联合疗法的临床优势,到 2031 年 relacorilant 在卵巢癌适应症上的销售额将达到 1.5 亿美元,有望成为该领域小众但关键的治疗选择,为患者提供新的治疗方案。
10 BGB-16673
百济神州研发的 BGB-16673 是一款靶向布鲁顿酪氨酸激酶(BTK)的嵌合式降解激活化合物(CDAC),核心适应症为复发或难治性慢性淋巴细胞白血病 / 小淋巴细胞淋巴瘤(CLL/SLL),采用每日一次口服的便捷给药方案。作为潜在首创性(first-in-class)蛋白降解剂,其最大技术突破在于可通过独特机制有效促进野生型及突变型 BTK 的降解,尤其能精准作用于疾病进展中常见的耐药性突变型 BTK,破解了传统 BTK 抑制剂易出现耐药的行业痛点。
扎实的临床数据为其疗效提供了有力支撑:I/II 期临床试验结果显示,BGB-16673 治疗 CLL/SLL 的客观缓解率(ORR)高达 94%,展现出优异的抗肿瘤活性。当前,BTK 抑制剂已在 CLL/SLL 主要市场治疗药物销售额中占据主导地位,而 BGB-16673 凭借 “降解而非抑制” BTK 的独特作用机制,不仅能覆盖传统 BTK 抑制剂的治疗人群,还能惠及耐药患者,有望进一步巩固 BTK 靶向疗法在该领域的核心优势,助力其在 2034 年前持续稳居 CLL/SLL 治疗领域的龙头地位。
作为本土药企自主研发的创新药,BGB-16673 的研发进展彰显了中国药企在蛋白降解领域的技术突破。科睿唯安报告对其市场潜力持乐观态度,预测 2031 年该药物在 G7 市场的销售额有望达到 11.9 亿美元,将成为百济神州全球化布局的重要支撑,同时为复发或难治性 CLL/SLL 患者带来全新治疗选择。
11 Mezigdomide
百时美施贵宝(BMS)研发的 Mezigdomide 属于第二代 cereblon E3 泛素连接酶调节剂(CELMoD),核心适应症聚焦复发或难治性多发性骨髓瘤(MM),是该领域靶向治疗的重要进阶品种。其作用机制具备明确的创新性与精准性:通过特异性降解造血细胞发育及分化过程中的关键转录因子 Ikaros 和 Aiolos,同步实现抗骨髓瘤增殖与免疫调节的双重治疗效果,相较第一代 CELMoD 药物,在作用效率与靶向性上更具优势。
目前,Mezigdomide 的研发已进入关键阶段,两项全球性 III 期临床试验正在推进中,核心探索其与其他已获批疗法联合应用于晚期多发性骨髓瘤的疗效与安全性,旨在进一步提升治疗应答率与患者生存期。科睿唯安报告指出,这款药物有望实现对 BMS 旗下经典 MM 治疗药物瑞复美(来那度胺)的替代 —— 核心优势在于耐受性更优,能有效降低现有治疗中常见的不良反应风险,提升患者长期治疗的依从性,为复发或难治性 MM 患者提供更安全的治疗选择。
从市场前景来看,多发性骨髓瘤作为血液系统常见恶性肿瘤,存在持续的临床需求,尤其复发难治人群的治疗选择极为有限。基于其差异化的临床价值,报告预测 2031 年 Mezigdomide 在 G7 市场的销售额将达 14.7 亿美元,有望成为 BMS 在血液肿瘤领域的核心增长引擎,同时推动多发性骨髓瘤治疗进入更精准、更安全的靶向治疗新阶段。
结语
科睿唯安这份 Drugs to Watch™报告,不仅勾勒出 2026 年全球创新药研发的核心赛道与重磅候选药物格局,更折射出当下生物医药领域的发展趋势:肥胖代谢领域凭借 GLP-1 类药物的迭代创新持续爆发,肿瘤、自身免疫、神经疾病等领域则在靶向疗法、蛋白降解、多靶点协同等技术突破中不断挖掘未满足医疗需求,而罕见病、慢病领域的精准治疗也成为药企研发布局的重要方向。
从礼来、强生等跨国药企的管线深耕,到百济神州等本土药企的创新出海,再到各细分领域首款创新疗法的接连涌现,不难看出,临床价值导向与技术差异化创新已成为创新药从实验室走向市场、成为重磅品种的核心逻辑。而这些候选药物的后续临床进展、审批落地与市场表现,也将持续影响全球医药市场的竞争格局,为患者带来更多治疗新选择。
未来,随着临床试验的推进与研发技术的升级,更多兼具疗效与可及性的创新疗法有望问世,生物医药行业也将在持续的探索与突破中,为全球健康事业注入更多动力。我们也将持续关注全球创新药研发与市场动态,带来最新的行业资讯与深度解读。
来源:https://mp.weixin.qq.com/s/waNBoJEd_X0BjV-R2EpZtg
END
——北京植众德本知识产权代理有限公司——
本公司致力于为全球客户提供卓越、全方位的知识产权服务。自成立以来,我们已迅速发展成为一家在生物医药、医疗器械、高端制造、芯片半导体及人工智能等领域具有深厚实力的知识产权代理服务机构。我们的服务网络覆盖全国,并延伸至全球,为超过200家行业先进客户,提供高质量的知识产权支持。
【声明】
植众德本通过其官方网站http://www.meritsip.com/ 提供更多相关信息。本文内容由植众德本小编从公开网络平台收集,版权归植众德本所有。未经植众德本授权,任何单位或个人不得转载本文内容。已获授权的,应在授权范围内使用,并注明来源。对于任何侵犯版权或信息错误的情况,植众德本将及时进行处理,并追究相关法律责任。授权相关事宜请联系:meritsip@meritsandtree.com。

欢迎扫码,联系我们


















